Пример вступительного испытания по химии
№1
1) Напишите электронную формулу элемента аргон 18Ar. (1 балл)
2) Приведите примеры двух катионов и двух анионов с такой же, как у аргона, электронной конфигурацией, расположив их в порядке возрастания радиуса. (2 балла)
3) Напишите формулы любых двух соединений, составленных из перечисленных вами частиц. К каким классам (классу) веществ относятся данные соединения? (1 балл)
4) Какой тип химической связи между частицами в данных соединениях? Кристаллическую решетку какого типа они формируют, находясь в твердом агрегатном состоянии? (3 балла)
5) Образуют ли химические элементы перечисленных частиц высшие оксиды? Приведите примеры возможных высших оксидов данных химических элементов и укажите их характер (основный, амфотерный, кислотный, индифферентный). (3 балла)
№2
Напишите уравнения следующих реакций:
1) уравнение гидролиза той из солей, которая гидролизуется по катиону: Na2CO3, NaCl, АlCl3 (в молекулярном, полном и сокращенном ионном видах)
2) термическое разложение солей NH4NO3, (NH4)2S, NaHCO3
3) электролиз водного раствора Pb(NO3)2 (написание электродных процессов обязательно!)
(5 баллов)
№3
Какие два вещества вступили в реакцию и при каких условиях, если в результате образовались следующие соединения (указаны ВСЕ продукты реакции без коэффициентов)? Составьте уравнения химических реакций. Для расстановки коэффициентов в окислительно-восстановительных реакциях используйте метод электронного баланса:
… + … → CaSiO3 (1 балл) … + … → SO2 + Na2SO4 + H2O (1балл)
… + … → CuCl (2 балла) … + … → Ag2SO4 + SO2 + H2O (2 балла)
… + … → Na2CO3 + CO2 + N2 (3 балла) … + … → FeCl2 + I2 + HCl (3 балла)
№4
Медь массой 6,4 г растворили в избытке концентрированной серной кислоты. Газ, выделившийся при этом, пропустили через водный раствор сульфита натрия массой 504 г и массовой долей сульфита натрия 5%. Определите массовые доли солей в полученном растворе. (5 баллов)
№5
Осуществите цепочку превращений:
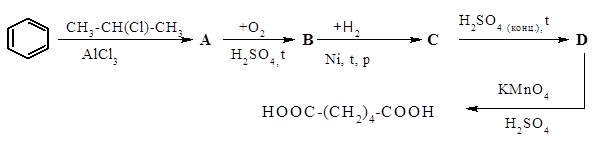
(1+1+1+2+3 = 8 баллов)
№6
Определите строение соединения C4H6O, которое дает реакцию «серебряного зеркала», существует в виде геометрических изомеров, при окислении водным раствором KMnO4 образует соединение С4Н8О4, при взаимодействии которого с раствором NaHCO3 выделяется газ. Напишите уравнения реакций, структурные формулы геометрических изомеров и назовите их. (5 баллов)
№7
В водном растворе уксусной и муравьиной кислот массой 190 г соотношение массы воды и массы обеих кислот составляет 3:2. При обработке этого раствора избытком гидрокарбоната натрия выделилось 33,6 л газа. Определите массовые доли каждой из кислот в растворе. (7 баллов)
Магистратура : pk.magistr@mipt.ru
Аспирантура : pk.phd@mipt.ru
Перевод, восстановление, иные вопросы : pk.mail@mipt.ru
